Фтордезоксиуридилат - Fluorodeoxyuridylate
 | |
| Имена | |
|---|---|
| Название ИЮПАК натрия; [(2R, 3S, 5R) -5- (5-фтор-2,4-диоксопиримидин-1-ил) -3-гидроксиоксолан-2-ил] метилгидрофосфат | |
| Другие имена FdUMP | |
| Идентификаторы | |
| |
3D модель (JSmol ) |
|
| ЧЭБИ |
|
| ЧЭМБЛ |
|
| ChemSpider |
|
| DrugBank |
|
| КЕГГ |
|
PubChem CID |
|
| UNII |
|
| |
| |
| |
| Свойства | |
| C9ЧАС11FN2NaО8п | |
| Молярная масса | 348.155 г · моль−1 |
Если не указано иное, данные для материалов приведены в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на инфобоксы | |
Фтордезоксиуридилат,[1] также известный как FdUMP, 5-фтор-2'-дезоксиуридилат или натриевая соль 5-фтор-2'-дезоксиуридина 5'-монофосфата, представляет собой молекулу, образованную in vivo из 5-фторурацила или 5-фтордезоксиуридина.
FdUMP действует как суицидальный ингибитортимидилатсинтаза (ТС). Ингибируя биосинтез дезоксинуклеотидов, FdUMP останавливает быстрое распространение быстрорастущих смертельных раковых опухолей, и поэтому он широко используется в качестве лечения рака.
В Фторурацил (5-FU), действует как субстрат во время части каталитический цикл, и только во время синтеза тимина из уридина, когда он объединяется с другими молекулами с образованием 5-FdUMP, вызывая необратимое ингибирование функций тимидилатсинтазы. Это ингибирование приводит к дисбалансу группирования нуклеотидов, останавливая ДНК синтез.[2]
Функция
5-ФУ и флоксуридин, предшественники FdUMP
Пролекарство 5-фторурацил (5-ФУ) был первым антиметаболит используется как ингибитор TS. Он проникает в клетку через тот же облегченный транспортный механизм, что и урацил, из-за аналогии между двумя молекулами (одинаковой формы и размера). Транспортер распознает 5-ФУ как эндогенную молекулу. Впоследствии урацил и 5-ФУ конкурируют за проникновение внутрь клетки, и именно молекула с наивысшей концентрацией войдет в большем количестве.
Чтобы 5-ФУ ингибировал TS по механизму действия, он должен быть сначала биоактивирован посредством ряда реакций:
- 5-FU в конечном итоге становится 5-FdUMP (активная форма препарата), то есть тот, который действительно будет распознаваться TS и, таким образом, сможет его ингибировать.
- Кроме того, путь биоактивации 5-ФУ такой же, как и путь эндогенного субстрата (урацила), с использованием того же ферменты биоактивировать себя.
С другой стороны, флоксуридин (5-FUdR) - другое пролекарство, которое также ингибирует TS; хотя его процесс биоактивации намного проще, чем 5-FU, поскольку он должен только фосфорилироваться, чтобы стать 5-FdUMP.

Механизмы ингибирования FdUMP
Однажды 5-ФУ или 5-FUdR пролекарства были биоактивированы с образованием FdUMP, они уже будут распознаваться ферментом TS. Когда это происходит, фермент претерпевает конформационные изменения, чтобы обеспечить объединение кофактора. 5,10-метилентетрагидрофолиевая[3] (5,10-CH2THF), который необходим для работы фермента. После объединения этого соединения реакция ингибирования начинается с другого механизма, который имеет место с урацилом.
Реакция начинается, когда цистеин остаток, присутствующий в активном участке фермента, атакует пиримидин в положении 2. Благодаря этому C5 атакует кофактор, образуя третичный комплекс, который включает фермент (TS), лекарство (5-FdUMP) и кофактор (5,10-CH2THF), что является необратимым.
После образования комплекса препарат теряет свою активность, поэтому его называют суицидным ингибитором, так как он выполняет свою функцию и остается инактивированным из-за образовавшихся ковалентных связей.[4]
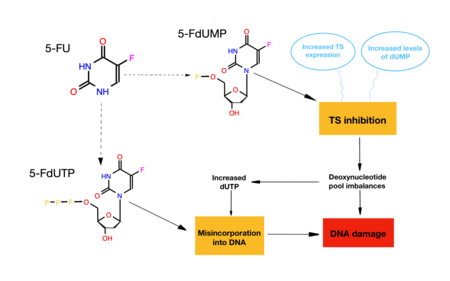
Последствия торможения TS
Это два различных способа вызвать гибель клеток в присутствии FdUMP:
- Когда TS ингибируется, среди прочего происходит снижение TMP, поскольку он не может быть синтезирован. Из-за этого dTTP (нуклеотид-предшественник ДНК) также не будет синтезироваться, что приведет к изменению баланса нуклеотиды, поэтому будут вариации в механизмах синтеза и восстановления ДНК из-за отсутствия тимина, вызывая смерть клетки.
- Если ингибирование TS не происходит, 5-FdUMP вместо ингибирования фермента может трифосфорилировать (5-FdUTP) и действовать как субстрат для ДНК-полимераза. Следовательно, он встраивается в ДНК и, поскольку он не является естественным субстратом, вызывает дестабилизацию молекулы и последующий разрыв цепи, действуя как мутаген и вызывая гибель клетки.
Изучение функции

Целью этого исследования было сравнить эффективность ингибирования TS различных молекул, включая FdUMP, 5FU и 5-фтор-2-дезоксиуридин (FUdR). Поэтому несколько линий клеток, включая дефицитные по тимидинкиназе (TK) и дефицитные по тимидилатсинтазе (TS), использовали для определения зависимости и специфичности TK в отношении ингибирования TS. Исследование могло показать, что FdUMP подавлял рост клеток с большей силой, чем 5FU.
Эти прямые ингибиторы также использовались, например, с Ралтитрекседом и Пеметрекседом. В тех же клеточных линиях эти ингибиторы на основе фолиевой кислоты также обладают большей силой, чем фторпиримидины (FP). Удивительно, но пеметрексед даже подавлял рост клеток с дефицитом TS.
Инкубация нуклеотидазы и фосфатазы привела к снижению цитотоксичности FdUMP, что означает, что лекарство может быть понижено в клетках.
В тесте на ингибирование TS (TSIA) in situ клетки FM3A с 0,5 мкМ FdUMP и 0,05 мкМ FdUMP экспонировали в течение 24 часов. Наконец, контроль TSIA снизился на 1-7%. Ингибирование активности нуклеотидазы и фосфатазы уменьшало эффект FdUMP, в то время как ингибирующий эффект был меньше в клетках, в которых отсутствовали ТК.
FdUMP может проникать как в интактные клетки, так и в активированные клетки, в которых дефосфорилирование уже началось. Подводя итог, был сделан вывод, что FdUMP может остановить сопротивление FUdR некоторых клеток, напрямую ингибируя TS.
Медицинские применения в клетках толстой кишки человека
- Конъюгат FA-FdUMP.[5] В настоящее время существует несколько связанных с фторпиримидином химиотерапия лечения, такие как 5-фторурацил (5-FU), которые ограничены химиорезистентностью к лекарствам. Но было показано, что конъюгация FdUMP с фолиевая кислота (FA) авторством фосфодиэфир связывание демонстрирует улучшенную цитотоксичность как для человека, так и для устойчивых к 5-ФУ колоректальных опухолевые клетки. Следовательно, конъюгат FA-FdUMP действительно очень полезен для лечения злокачественных опухолей, устойчивых к 5-ФУ.
- Аденокарцинома в клетках толстой кишки (повреждения ДНК).[6][7][8] При сравнении возможностей 5-FU и FdUMP в отношении клеток аденокарциномы толстой кишки человека было показано, что оба препарата могут индуцировать апоптоз, хотя их влияние на клеточный цикл прогрессия разная. С другой стороны, разница в моменте остановки клеточного цикла предполагает, что два препарата вызывают разные типы первичных повреждений ДНК, которые могут привести к активации разных контрольных точек и, следовательно, следовать разным путям репарации ДНК.
использованная литература
- ^ "Ingebook - BIOQUÍMICA 7ED - Con aplicaciones clínicas". www.ingebook.com. Получено 2019-10-24.
- ^ Собич, Юстина; Прокопович, Малгожата; Май, Петр; Вилк, Петр; Зелински, Збигнев; Frączyk, Tomasz; Роде, Войцех (2019-10-15). «Катализируемая тимидилатсинтазой, тетрагидрофолат-зависимая самоинактивация 5-FdUMP». Архивы биохимии и биофизики. 674: 108106. Дои:10.1016 / j.abb.2019.108106. ISSN 1096-0384. PMID 31520592.
- ^ "Мэтьюз / ван Холд / Ахерн, третье издание". www.uaz.edu.mx. Получено 2019-10-24.
- ^ К. Мэтьюз, Кристофер (январь 1963 г.). «Ингибирование фаг-индуцированной тимидилатсинтетазы 5-фтордезоксиуридилатом».
- ^ Лю, Цзиньцянь; Колар, Кэрол; Лоусон, Терренс А .; Гмайнер, Уильям Х. (2001-08-01). «Направленная доставка лекарств к химиорезистентным клеткам: дериватизация фолиевой кислоты из FdUMP [10] усиливает цитотоксичность в отношении 5-ФУ-устойчивых клеток колоректальных опухолей человека». Журнал органической химии. 66 (17): 5655–5663. Дои:10.1021 / jo005757n. ISSN 0022-3263. PMID 11511236.
- ^ Лю, Цзиньцянь; Колат, Джефф; Андерсон, Джеймс; Колар, Кэрол; Лоусон, Терренс А .; Талмадж, Джеймс; Гмайнер, Уильям Х. (1999-10-01). «Положительное взаимодействие между 5-FU и FdUMP [10] в ингибировании пролиферации клеток колоректальной опухоли человека». Разработка антисмысловых и нуклеиновых кислот. 9 (5): 481–486. Дои:10.1089 / oli.1.1999.9.481. ISSN 1087-2906. PMID 10555156.
- ^ Матуо, Рената; Соуза, Фабрисио Гармус; Escargueil, Alexandre E .; Гривичич, Ивана; Гарсиа-Сантос, Даниэль; Чиес, Хосе Артур Бого; Саффи, Дженифер; Ларсен, Аннет К .; Энрикес, Жоао Антонио Пегас (2009). «5-Фторурацил и его активный метаболит FdUMP вызывают повреждение ДНК в клеточной линии аденокарциномы толстой кишки SW620 человека». Журнал прикладной токсикологии. 29 (4): 308–316. Дои:10.1002 / jat.1411. ISSN 1099-1263. PMID 19115314.
- ^ Gmeiner, William H .; Скрадис, Алан; Пон, Ричард Т .; Лю, Цзиньцянь (1999-06-01). «Цитотоксичность и толерантность in vivo к FdUMP [10]: новый пролекарство ингибиторного нуклеотида TS FdUMP». Нуклеозиды и нуклеотиды. 18 (6–7): 1729–1730. Дои:10.1080/07328319908044836. ISSN 0732-8311.
